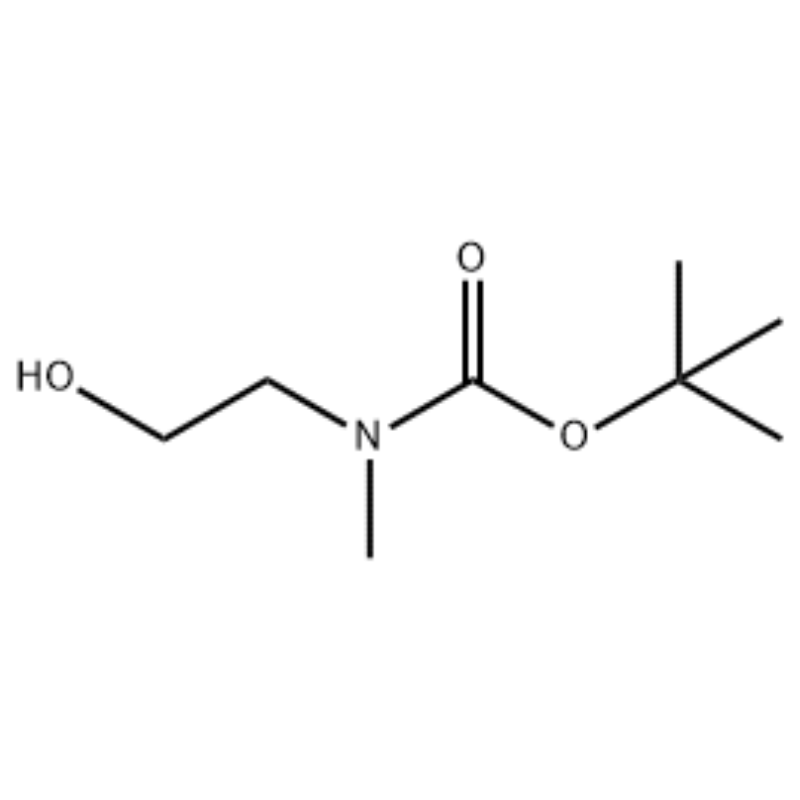
A una solución de 2-(metilamino)etanol (500 mg, 0,53 ml, 6,66 mmol) en CH2Cl2 (20 ml) se le añadió Boc2O (1,48 g, 6,79 mmol), seguido de agitación a temperatura ambiente durante 1 hora.La solución de reacción se extrajo con salmuera y CH2Cl2.La capa orgánica así obtenida se secó sobre MgSO4 y se filtró.Luego, el filtrado se concentró al vacío para obtener el compuesto objeto (aceite incoloro, cuantitativo);RMN 1H (200 MHz, CDCl3) delta 3,74 (q, J= 10,5, 5,2 Hz, 2H) 3,25 (t, J= 5,2 Hz, 2H) 2,91 (s, 3H) 1,45 (s, 9H);espectro de masas m/e (intensidad relativa) 144 (20) 102 (24) 57 (70) 44 (100).
Ejemplo 38;N1-(3-fluoro-4-(2-(1-(2-(metilamino)etil)-1H-imidazol-4-il)tieno[3,2-b]piridin-7-iloxi)fenil)-N3 -(2-metoxifenil)malonamida (96);Paso 1: 2-hidroxietil(metil)carbamato de terc-butilo (97) (J. Med. Chem., 1999, 42, 11, 2008) A una solución de 2-(metilamino)etanol (5,0 g, 67 mmol) en Se añadió THF (50 ml) a temperatura ambiente, Boc2O (15,7 g, 72 mmol) y la mezcla de reacción se agitó a temperatura ambiente durante 4 horas.La mezcla de reacción se concentró hasta sequedad y el compuesto del título 97 se usó directamente en la siguiente etapa sin purificación adicional (11,74 g, rendimiento del 100 %).EM (m/z): 176,2 (M+H).
Preparación de 1-2-[4-Bromo-2-(4-oxo-2-ftiotaioxo1hiazolidin-5-ilidenmefliil)fenoxi]efliil-3-efliil-1-metilurea (Compoiotamd 161) Paso 1: Síntesis de t-butil2- carbamato de hidroxietilmetilo;A una solución de 2-(metilamino)etanol (500 mg, 0,53 ml, 6,66 mmol) en CH2Cl2 (20 ml) se le añadió BoC2O (1,48 g, 6,79 mmol), seguido de agitación a temperatura ambiente durante 1 hora.La solución de reacción se extrajo con salmuera y CH2Cl2.La capa orgánica así obtenida se secó sobre MgSO4 y se filtró.Luego, el filtrado se concentró al vacío para obtener el compuesto objeto (aceite incoloro, cuantitativo); 1HNMR (200 MHz, CDCl3) delta 3,74 (q, J= 10,5, 5,2 Hz, 2H) 3,25 (t, J= 5,2 Hz, 2H) 2,91 (s, 3H) 1,45 (s, 9H);espectro de masas m/e (intensidad relativa) 144 (20) 102 (24) 57 (70) 44 (100).
Se disolvió 2-(metilamino)etanol (90,1 g, 1,2 mol) en 1,2 l de cloruro de metileno y se le añadió lentamente BoC2O (218 g, 1 mol) mientras se agitaba a 0ºC, seguido de temperatura ambiente durante 3 horas.La mezcla de reacción se lavó secuencialmente con 700 ml de una solución acuosa de cloruro de amonio saturado y 300 ml de agua.La mezcla lavada se deshidrató usando sulfato de sodio anhidro y se concentró a presión reducida, para obtener el compuesto (a) (175 g, 1 mol, 100%) como un aceite sin color. TLC: Rf = 0,5 (50% EtOAc en Hex) visualizado con tinción Ce-Mo RMN 1H (600 MHz, CDCl3) delta 1,47 (s, 9H), 2,88 (br s, IH), 3,41 (br s, 2H), 3,76 (br s, 2H).
Se disolvieron 90,1 g (1,2 moles) de 2-(metilamino)etanol en 1,2 l de cloruro de metileno, se añadieron lentamente a esto 218 g (1 mol) de Boc2O mientras la solución resultante se agitaba a 0ºC y la solución resultante se agitaba a temperatura ambiente durante 3 horas.La mezcla de reacción se lavó secuencialmente con 700 ml de una solución acuosa saturada de cloruro de amonio y 300 ml de agua, se deshidrató usando sulfato de sodio anhidro y luego se concentró a presión reducida para obtener 175 g (1 mol) de un compuesto de aceite acrómico protegido por el Grupo Boc (rendimiento: 100%).RMN 1H (600 MHz, CDCl3) delta 7,84 (br s, 2H), 7,76 (br s, 2H), 4,34 (d, J = 15,0 Hz, 2H), 3,63 (br s, 2H), 3,04 (d , J = 15,0 Hz, 3H), 1,46 (d, J = 16,2 Hz, 9H) Se disolvieron 90 g (0,514 mol) del compuesto obtenido en 1,5 l de tetrahidrofurano, 88,0 g (539 mol) de N- A esto se le añadieron hidroxiftalimida y 141 g (0,539 mol) de trifenilfosfina, se le añadieron lentamente 106 ml (0,539 mol) de azodicarboxilato de diisopropilo mientras se agitaba la solución resultante a 0ºC, y la solución resultante se agitó durante 3 horas mientras se elevaba su temperatura. a temperatura ambiente.Después de concentrar la mezcla de reacción a presión reducida, se le añadieron 600 ml de éter isopropílico, la solución resultante se agitó a 0ºC durante 1 hora y se filtró óxido de trifenilfosfina de tipo sólido blanco.El sólido se lavó con 200 ml de éter isopropílico enfriado a 0ºC y se recogió con el primer filtrado, y el filtrado resultante se concentró a presión reducida para obtener 198 g de una mezcla de Compuesto XX e hidrazodicarboxilato de diisopropilo en una proporción de mezcla del 10 al 15%. (rendimiento: 120%).RMN 1H (600 MHz, CDCl3) delta 7,84 (br s, 2H), 7,76 (br s, 2H), 4,34 (d, J = 15,0 Hz, 2H), 3,63 (br s, 2H), 3,04 (d , J = 15,0 Hz, 3H), 1,46 (d, J= 16,2 Hz, 9H)
 Edificio 12, No 309, South 2nd Road, Zona de Desarrollo Económico, Distrito de Longquanyi, Chengdu, Sichuan, China.
Edificio 12, No 309, South 2nd Road, Zona de Desarrollo Económico, Distrito de Longquanyi, Chengdu, Sichuan, China. amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com
amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com +86 (028) 84841969
+86 (028) 84841969 +86 135 5885 5404
+86 135 5885 5404



















.png)


